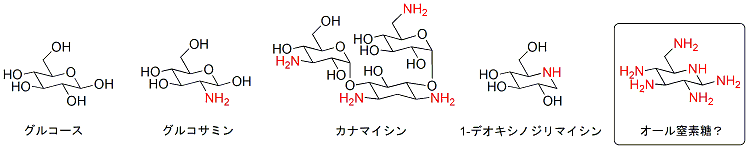
糖はポリアルコール構造をもつ天然分子ですが、天然にはこの糖の構造の酸素の一部を窒素で置き換えた分子があります。たとえば、グルコースの2位のヒドロキシ基をアミノ基で置換したグルコサミンは、細胞表層糖鎖や構造多糖の単位として重要な化合物ですし、抗菌性抗生物質であるカナマイシンのような窒素を複数含むグリコシド分子や、強力なグルコシダーゼ阻害活性をもつ1-デオキシノジリマイシンのようなピラノース環内に窒素をもつ分子もあります。このように糖の窒素置換体(アザ糖)には多数の興味深い生理活性を示す分子が知られています。

さて、それでは糖の酸素をすべて窒素で置換してしまったらどうでしょう。たとえば上図右端のオール窒素グルコースのような分子です。こうなるとまさにおもしろ化合物というべきでしょう。ここまで徹底した分子はこれまでに知られていませんが、どういう物性あるいは生理活性を示すのか興味が持たれます。このたび、この全窒素糖の初の合成に挑んだ報告がなされました。1)
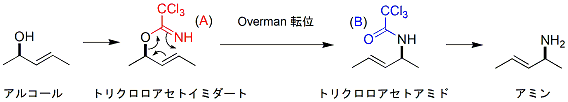
こういう珍妙な分子をいったいどうやって合成したらよいでしょう。たくさんの不斉中心をコントロールして一から作るのは大変そうなので、糖を原料としてヒドロキシ基をそのままアミノ基に変換できればよさそうですが、そう簡単にはいきません。
そこで著者らはアリルアルコールのトリクロロアセトイミダートエステルを、[3,3]-シグマトロピー転位によってトリクロロアセトアミドに変換するOverman転位反応の利用を考えました。この反応は6員環遷移状態を経るために、元のアルコールの根元の立体化学がアミノ基の根元に保持されるという利点もあります。ただし、アリル転位を伴うために原料のアルコールと生成物のアミンでは結合する炭素の位置が2つずれてしまいます。ポリアルコールである糖にこの反応を応用した場合、そこがどう表れるかが問題です。
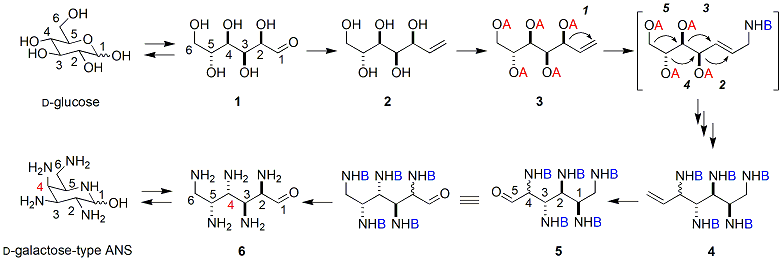
とりあえずD-グルコース(1)で考えてみましょう。まず、グルコースの1位のアルデヒドをWittig反応によって末端オレフィン(2)とします。次に2のすべてのアルコールをトリクロロアセトイミダート化し、3とします(図ではトリクロロアセトイミダート基をAと略記)。これをOverman転位反応に供すると、まず1回目の転位が起きてカッコ内のモノアセトアミド体に変換されます(図ではトリクロロアセチル基をBと略記)。二重結合がひとつずれるので、こんどは次のアルコールが転位することができ、というふうに順次反応がパタパタと進み、最終的に図の5回の転位を経て逆側に末端オレフィンが移ったポリアミド体(4)になります。このとき、立体化学はすべて保持されて転位しますが、最後の6位は一級アルコールなので、この部分のみジアステレオマー混合物になります。生成物の二重結合を酸化的に切断してアルデヒド(5)にすれば、元の糖の炭素鎖が逆転した形の窒素糖構造ができあがります。
問題の立体化学ですが、鎖を左右ひっくり返して炭素番号を振り直し、元の鎖と並べてみると、2位がラセミ化、3位と5位は保持、4位が反転していることがわかります。2位はアルデヒドの隣接位なので容易に安定な元の立体配置に変換可能です。ということは、D-グルコースから出発してできた全窒素糖(6)は4位のみが反転したすなわちD-ガラクトース型分子ということになります。著者らはこの生成物をD-galactose-type ANS (all-nitrogenated sugar)と命名しています。
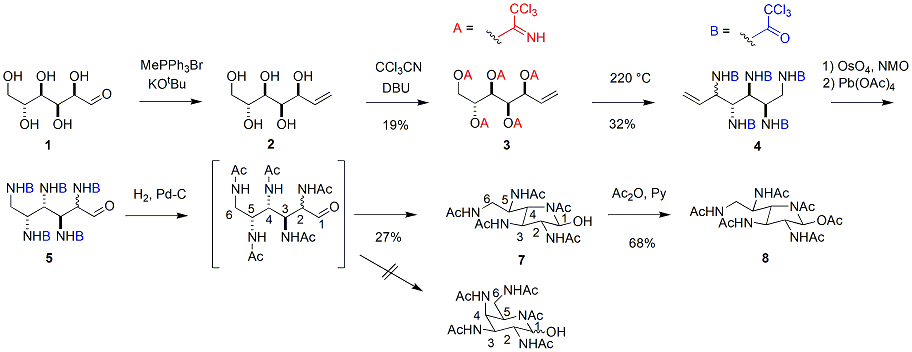
それでは実際の反応を見てみましょう。まずD-glucose(1)をWittig反応でオレフィン化(2)した後、塩基性条件下すべてのヒドロキシ基をトリクロロアセトニトリル付加によってイミダート体(3)とします。この2段階の収率は19%でした。次にこの3を220 ℃に加熱して連続的なOverman転位を起こさせると、32%の収率で一気にペンタトリクロロアセトアミド体(4)に変換されます。このとき左端の不斉中心に関してジアステレオマー混合物(2:1)となります。末端オレフィンを四酸化オスミウムでジオールに酸化してから四酢酸鉛で酸化的に開裂してアルデヒド体(5)とします。このままでは置換基の立体障害で環化しないので、トリクロロアセチル基を加水素分解によってアセチル基に変換すると、ヘミアセタール環化が起こって5員環フラノース型の7となります(4からここまでの収率27%)。このとき、なぜか6員環のピラノース型閉環体はまったく得られません。アノマー位をアセチル化するとperacetyl D-galactofuranose-type ANS(8)のできあがりです。同じ方法を使ってD-ガラクトースから出発して、D-グルコース型ANSの合成も達成しています。
アノマー位のみ酸素が残っていますが、この位置は容易にアミンに変換可能であり、また配糖体のように誘導体化した場合は失われる部分なので、まあ完全窒素化糖といっても過言ではないでしょう。ただし8はアミノ基がすべてアセチル化されているので、ぜひとも脱保護して遊離のアミノ体にはしたいところです。
実際に著者らは別途合成したアセチル化 D-アラビノフラノース型ANSについて、二級アミド部分のみBoc化、塩基性加水分解、脱Boc化によって遊離のアミノ基への変換をしていますが、この方法では環内窒素の三級アミドをはずすことができず、ここだけアセチル基が残ってしまっています。論文には触れられていませんが、アミドははずしにくい保護基であり、遊離のポリアミノ体分子はあまり安定ではないでしょうから、完全脱保護はうまくいってないのでしょう。
また、できれば通常のヘキソースの存在形態である6員環ピラノース型分子もつくりたいところです。アラビノースのようなペントース型分子の合成時には、閉環時にフラノース型とピラノース型の両閉環体が得られているので、ヘキソースでピラノース型がまったく得られないのは、理由は不明ながら残念ですね。
最後に、著者らはアセチル化 D-アラビノフラノース型ANSをコレステロールに縮合させた配糖体をつくったところ、弱いながら細胞毒性が見られたことを記載しています。アセチル化されていること、フラノース型であることを考えると、天然の配糖体分子の完全窒素化アナログとはいいがたいので、このあたりの検討はまだまだこれからというところでしょう。
1) Y. Okuyama, M. Kidena, E. Kato, S. Kawano, K. Ishii, K. Maie, K. Miura, S. Simizu, T. Sato, and N. Chida, Angew. Chem. Int. Ed. 2020, doi.org/10.1002/anie.202015141.